免疫细胞+趋化因子,这么做免疫你也能轻松发顶刊!
来源:小张聊科研平台的“ 课题指南针”公众号,微信公众号搜索“ 课题指南针”即可关注/扫描关注见文末
持续火爆的肿瘤免疫已经有无数篇文章了,一般的研究要么靶向免疫细胞,要么靶向趋化因子。
那么如果我们靶向的是趋化因子+免疫细胞是不是会有1+1>2的效果呢?
Treg(Regulatory cells,调节性T细胞)是一类具有显著免疫抑制作用的免疫细胞,有大量的文献已经报道过Treg直接或间接抑制CD8+T(细胞毒性T淋巴细胞)或DC(树突状细胞)的功能,但是Treg如何被招募以及发挥抑制抗肿瘤免疫的机制尚未研究清楚。
免疫细胞在循环系统和组织器官间定向迁移离不开趋化因子与其受体的相互作用,那么Treg被招募和激活是否与趋化因子相关呢?
近日,加利福尼亚大学伯克利分校的研究人员在Cell子刊Immunity期刊发表《CXCR3 expression in regulatory T cells drives interactions with type I dendritic cells in tumors to restrict CD8+ T cell antitumor immunity》的研究文章,他们发现趋化因子受体CXCR3的表达,是肿瘤内Treg细胞积累和激活的关键。

具体而言,他们发现树突状细胞可以招募表达CXCR3的Treg细胞,与之相互作用并抑制其抗原提呈能力,导致CD8+T细胞无法被启动,从而限制抗肿瘤免疫反应,提示CXCR3+Treg是促进癌症免疫治疗的治疗靶点。
趋化因子千千万,为何就聚焦于CXCR3呢?
通过大量的文献阅读,研究人员注意到CXCR3表达于多种免疫细胞,包括Treg、CD8+T细胞等,CXCR3可以被DC1来源的趋化因子CXCL9和CXCL10所招募,从而促进CD8+ T细胞和DC1在空间上拉近,实现细胞互作并被激活,发挥抗肿瘤免疫作用。
再结合Treg也表达CXCR3,因而研究人员从思考是否可能存在以下可能:CXCR3+Treg也会和CD8同时被招募到DC1周围,进而在空间上减少CD8和DC1的近距离互作,减少CD8+T细胞的激活呢?
说干就干,研究人员对于上述猜想从以下三个方向逐步展开研究:

- 在诸多肿瘤表型发现基本现象:相比于淋巴组织,MC38(结肠癌)、EL4(胸腺淋巴瘤)和9464D(神经母细胞瘤)等肿瘤中CXCR3+Treg细胞增多,并且表现出活化的表型。
- 对该表型背后的免疫机制进行深入研究:Treg细胞的CXCR3消融增加DC1s的肿瘤抗原特异性交叉呈递,同时增加肿瘤CD8+T细胞的启动和再激活,最终阻止肿瘤的进展。
- 在动物层面探究该发现的治疗意义:Treg细胞CXCR3消融与抗PD-1检查点阻断免疫疗法相结合,显著降低肿瘤进展。
现象
研究人员首先检测了趋化因子受体CXCR3是否在Treg细胞上表达以响应来自不同组织的肿瘤。
他们发现在结肠癌、胸腺淋巴瘤、神经母细胞瘤等肿瘤模型中CXCR3在Treg细胞上的表达随着肿瘤的临近而增加,CXCR3+Treg在外周淋巴结中的表达可以忽略不计,但CXCR3+Treg细胞在肿瘤引流淋巴结和肿瘤中的表达比例增加。
此外,研究人员还注意到Treg细胞和CD8+T细胞的浸润数量呈正相关,这表明Treg细胞上CXCR3的表达可能对调节CD8+T细胞的抗肿瘤反应很重要。此外,他们还注意到与CXCR3- Treg细胞相比,CXCR3+Treg处于高激活状态。
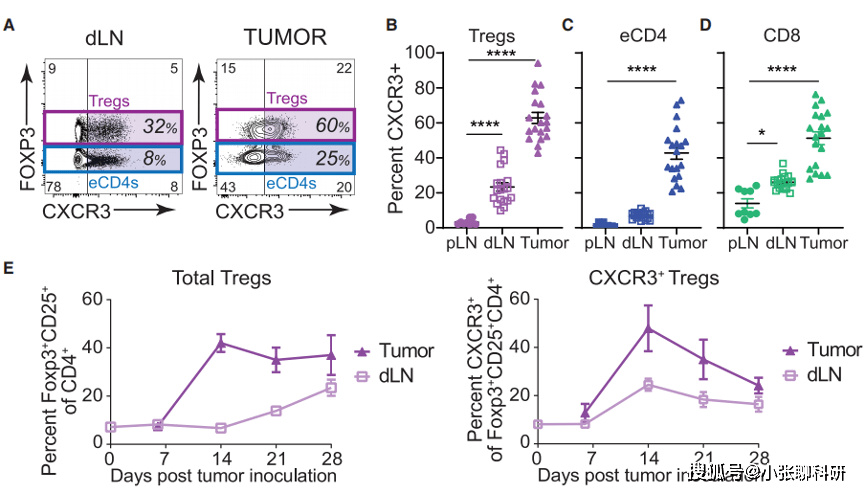 图1. 肿瘤中CXCR3+Treg细胞增多,并处于高活化状态
图1. 肿瘤中CXCR3+Treg细胞增多,并处于高活化状态
机制
接下来研究人员构建了Treg特异性CXCR3缺陷小鼠以探究CXCR3在Treg发挥免疫功能中的作用,他们发现相比于对照组,Treg特异性CXCR3缺陷小鼠在所有三种癌症模型(MC38、EL4和9464D)中都表现出肿瘤生长延迟,这表明Treg细胞上CXCR3的表达在促进癌症进展中具有关键作用。
为了探究其中的更深层机制,研究人员评估了Treg特异性CXCR3缺陷小鼠和正常小鼠肿瘤内CD8+T细胞的反应,他们发现在所有肿瘤模型中Treg特异性CXCR3缺陷小鼠瘤内CD8+T细胞的频率增加,而抗体介导的CD8+T细胞的耗尽逆转了Treg特异性CXCR3缺陷小鼠中观察到的肿瘤生长抑制,说明Treg细胞上CXCR3的缺失与肿瘤中抗肿瘤CD8+T细胞数量的增加相关,也就是说CXCR3+Treg细胞通过抑制肿瘤中抗肿瘤CD8+T细胞的积累来促进癌症。
 图2. 敲除Tregs中的CXCR3会促进抗肿瘤免疫
图2. 敲除Tregs中的CXCR3会促进抗肿瘤免疫
此外,研究人员还发现Cxcr3缺陷Treg细胞在肿瘤组织中积累的能力受损,趋化因子CXCL9对CXCR3+ Treg细胞的定位尤为重要,CXCR3+ Treg细胞与DC1s的共定位限制了肿瘤抗原的DC1交叉呈递,阻碍了抗肿瘤CD8+T细胞对癌症进展的控制。
治疗意义
进一步,研究人员对上述发现的治疗意义进行了探究,他们发现Treg特异性CXCR3缺陷与抗PD-1检查点阻断免疫疗法相结合,会显著抑制肿瘤进展。
在Treg特异性CXCR3缺陷小鼠中,肿瘤浸润的CD8+T细胞仍表达高水平的PD-1,当其在肿瘤进展的第7天开始接受抗PD-1治疗时,相比于对照组小鼠,Treg特异性CXCR3缺陷小鼠的肿瘤生长抑制更为明显,这提示CXCR3+Treg可能是促进癌症免疫治疗的新型治疗靶点。
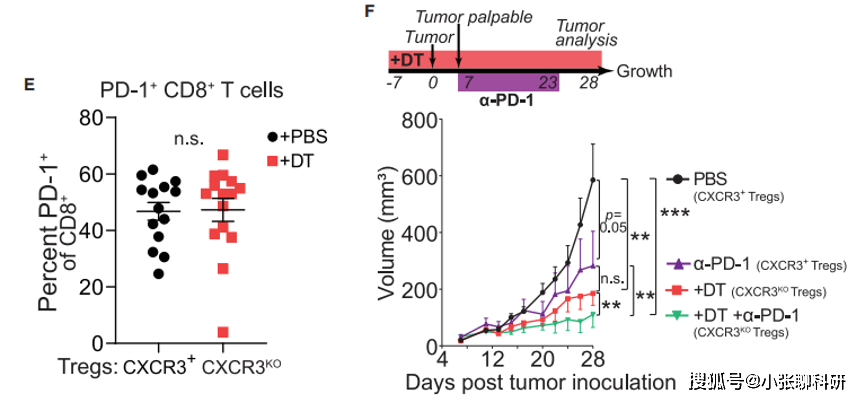 图3. Treg特异性CXCR3敲除结合抗PD-1检查点阻断免疫疗法显著抑制肿瘤进展
图3. Treg特异性CXCR3敲除结合抗PD-1检查点阻断免疫疗法显著抑制肿瘤进展
文章总结
虽然这篇文章对于免疫治疗提出了一个很有希望的新型靶点,但是值得注意的是CXCR3在其他表达CXCR3的免疫细胞(如T细胞和NK细胞)可能会影响对CXCR3总的阻断效果。
但是这篇文章还是凭借明显的现象+大量的机制研究成功发表于免疫学顶刊,不可否认的是,医学科研本来就是千丝万缕,一篇文章如果能清清楚楚地说明一个问题就已经很不错了!
简单看来,本文是从明星免疫细胞Treg入手,探究了明星趋化因子CXCR3在其活化、积累、发挥免疫抑制过程中的重要作用。
免疫细胞千千万,趋化因子也不少,两者相遇会迸出什么样的火花呢!
再退一步来说,Treg细胞中的趋化因子也不止CXCR3,CXCR3也不止在Treg上表达。
在肿瘤免疫治疗火热的浪潮中,你也能找到属于自己的免疫细胞+趋化因子,轻松发顶刊!
原文链接:https://mp.weixin.qq.com/s/5SJVb8HetMFMu3rnnVZ5LA
